Mycoplasma bovis: feiten, risico’s en aanpak
Mycoplasma bovis is een bacterie die bij menig veehouder bekend is, vaak omwille van hun eigen (negatieve) ervaring. Het is een ziekteverwekker die wereldwijd problemen veroorzaakt. Ook in Vlaanderen groeit de bezorgdheid. Mycoplasma bovis behoort dan ook tot een van de grootste uitdagingen binnen de sector. Het Project MycoSTOP werkt aan een betere aanpak ervan.
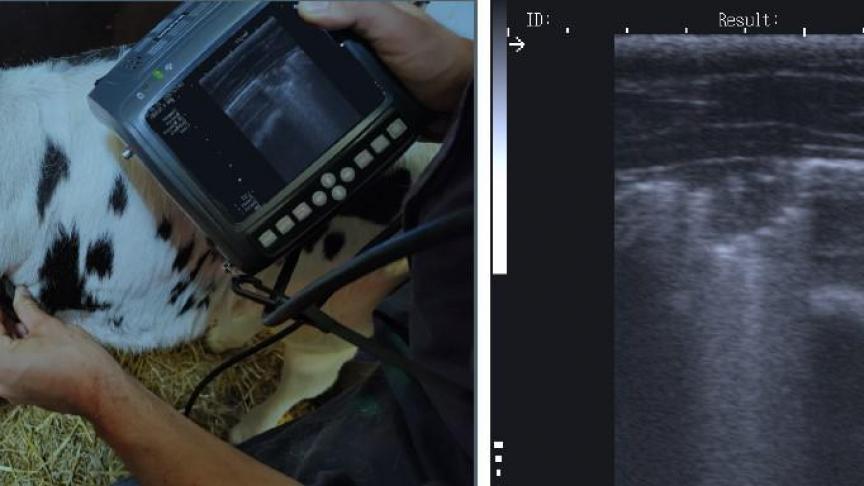
De universiteit Gent (UGent), Dierengezondheidszorg Vlaanderen (DGZ), Inagro en Hooibeekhoeve sloegen de handen in elkaar voor het project MycoSTOP. MycoSTOP heeft als doel het ontwikkelen van betere testprotocollen voor de aankoop en afvoer van dieren, alsook ter ondersteuning van opvolging van kalvergezondheid door middel van longechografie. Dit is een innovatie die naar de praktijk werd gebracht via het Vlaio-project PneumoNEE.
Over mycoplasma wordt veel geschreven en gesproken en blijkt er veel verwarring te bestaan. Als onderdeel van het project MycoSTOP sommen we dan ook enkele feiten op die gebaseerd zijn op het meest recente onderzoek.
Wat is ‘Mycoplasma bovis’?
Mycoplasma bovis (hierna kortweg M. bovis genoemd) is een kleine bacterie die zowel bij melk- als vleesvee kan leiden tot ziekte en zelfs sterfte. De infectie manifesteert zich vooral als longontsteking (pneumonie), gewrichtsontsteking (arthritis) en oorontsteking (otitis) bij kalveren en als gewrichtsontsteking en ongeneeslijke uierontsteking (mastitis) bij adult vee. Bovendien zorgt de chronische aard van de ziekte voor een verhoogd antibioticagebruik en een verhoogde kans op afvoer van besmette dieren. Verschillende studies toonden namelijk aan dat chronische niet-genezende longontstekingen bij kalveren op lange termijn heel schadelijke effecten kunnen geven, zoals een verminderde dagelijkse groei en een verminderde melkproductie bij melkvee.
Komt mycoplasma nu meer voor?
De eerdergenoemde klinische ziektebeelden vormen slechts het topje van de ijsberg. In België zien we de laatste jaren een stijgende trend in het voorkomen van mycoplasma. Zo toonde een eerdere studie uit 2019 aan dat M. bovis betrokken is bij maar liefst 33,3% van de uitbraken van luchtweginfecties in België. Onderzoeken we tankmelk door middel van antistoftesten of PCR, dan blijkt opnieuw 31,8% van de melkveebedrijven positief te testen op M. bovis. Gemiddeld is dus ongeveer 1 op 3 van de Vlaamse bedrijven positief voor M. bovis, ook zonder klinische problemen zijn. Cijfers bij Arsia (de Waalse tegenhanger van DGZ) tonen gelijkaardige resultaten.
Deze hoge cijfers zijn deels te verklaren doordat we waarschijnlijk met een hoge infectiegraad te maken hebben, maar ook door het feit dat we heel veel gaan testen. Deze stijgende trend doet zich niet alleen voor in België, maar ook in onze buurlanden zoals Frankrijk en Nederland en in Scandinavische landen zoals Finland en Denemarken. In 2017 werd ook Nieuw-Zeeland getroffen, dat voordien als vrij werd bestempeld.
Hoe raakt mijn bedrijf besmet en hoe verspreidt mycoplasma zich?
De meest gekende risicofactor voor introductie van M. bovis in de kudde is aankoop van recent geïnfecteerde dieren of langdurige uitscheiders. Eenmaal binnen op het bedrijf kan deze bacterie zich razendsnel verspreiden. Tussen koeien gebeurt dit meestal via neus-neus-contact of via het melkstel. Verder zijn het gebruik van een dekstier en de afwezigheid van een aparte afkalfbox risicofactoren voor besmetting met M. bovis. Besmetting van kalveren gebeurt voornamelijk door onderling contact of door het opnemen van geïnfecteerde melk. Het risico op besmetting via de eigen biest is beperkt, maar zeker niet onbestaande. Ook indirecte overdracht via materialen of personen is mogelijk.
Wat M. bovis zo verraderlijk maakt, is dat ze in de cellen van de gastheer kan kruipen zonder dat dieren er ziek van worden. Een koe kan maandenlang drager zijn zonder zichtbaar ziek te zijn, waardoor de kiem zich ongemerkt in de kudde kan gaan verspreiden.
Wat houdt de infectie op bedrijfsniveau in stand?
We merken dat steeds meer melkveebedrijven zich laten testen op de aanwezigheid van M. bovis of van antistoffen in de tankmelk. Dit kan een vals gevoel van veiligheid geven, omdat juist de kalveren de motor van de infectie zijn. Het zijn met andere woorden vaak de kalveren die de infectie in stand houden op het bedrijf. Vermoedelijk kan een klein deel van deze kalveren drager worden van de bacterie. Hoe groot dit aandeel precies is, is momenteel nog onduidelijk, maar eerdere studies suggereren dat het om een zeer laag percentage gaat.
Welke behandeling resulteert in de beste genezing?
Zichtbaar zieke kalveren zijn slechts het topje van de ijsberg. Voor elk ziek dier, zijn er 3 subklinisch aangetast. Dit betekent dat deze dieren nauwelijks ziekteverschijnselen vertonen, maar wel ongezien de kiem over het bedrijf kunnen gaan spreiden.
Een betrouwbare manier om deze verborgen gevallen op te sporen, is snelscan longechografie (quick thoracic ultrasound - qTUS). Met deze techniek kan een dierenarts in amper 1 à 2 minuten vaststellen of er sprake is van pneumonie (longontsteking) en kan hij een onderscheid maken met ontstekingen van de bovenste luchtwegen. Gezien pneumonie vaak bacterieel van oorsprong is, is het behandelen van dieren met een longontsteking met antibiotica een logische vervolgstap.
Toch is dit vaak minder eenvoudig dan gedacht. Zo is M. bovis van nature ongevoelig voor penicilline-achtigen en trimethoprimsulfonamiden. Eerstelijnsproducten, zoals florfenicol en oxytetracycline, lijken betere alternatieven, vooral bij vroege detectie. Dit blijkt ook uit een studie waarbij longechografie werd gebruikt om de behandeling te begeleiden tijdens een uitbraak van M. bovis op een gesloten vleesveebedrijf. Hierbij werd aangetoond dat dankzij longechografie en gerichte behandeling meer dan 95% genezing bereikt werd na 7 dagen, met halvering van het antibioticagebruik. Bovendien werd door individueel te behandelen bijna de helft minder antibiotica gebruikt dan bij een standaard groepsbehandeling van 7 dagen. Longechografie maakt zo een vroegtijdige diagnose mogelijk, wat leidt tot een hogere kans op genezing en een lager antibioticagebruik. Binnen het project wordt deze techniek, in combinatie met diagnostiek, dan ook ingezet om meer inzicht te krijgen in het verloop van behandelingen en om na te gaan of genezen dieren ook effectief stoppen met het uitscheiden van de kiem.
Wat doen bij menginfecties?
Helaas is de behandeling niet altijd zo rechtlijnig. Het genezingspercentage kan sterk variëren naargelang de weerstand van het kalf en het optreden van menginfecties met andere virussen of bacteriën. Deze menginfecties verergeren niet alleen het ziekteproces, maar zorgen er ook voor dat de ingestelde behandeling vaak onvoldoende effectief is. Naast de natuurlijke resistentie, komt verworven resistentie (onder andere tegen macroliden) ook voor. Door het ontbreken van een duidelijk referentiekader is het voor dierenartsen echter vaak lastig om onmiddellijk het meest effectieve antibioticum te gaan inzetten. Ons advies hierbij is om kalveren systematisch met longechografie op te volgen en om bij therapiefalen longspoelingen uit te voeren. Op die manier kan beter worden vastgesteld of resistentie een rol speelt en/of bijkomende infecties de overhand hebben genomen.
Hoe kan ik een individueel dier testen bij aankoop?
De meest duurzame oplossing blijft het effectief bestrijden van de infectie. In Nieuw-Zeeland gaat men hierin heel ver: zodra een dier positief test op antistoffen, moet het onmiddellijk worden geruimd. Deze aanpak is zeer radicaal en onrealistisch voor de huidige situatie in België. Zoals eerder aangehaald, vormt de aankoop van dieren het grootste gevaar. Momenteel kan enkel op antistoffen getest worden, die enkel iets zeggen over vroegere besmettingen. Of dieren nog actief geïnfecteerd zijn en dus nog steeds besmettelijk zijn, is met de huidige antistoftest niet duidelijk. Dit zorgt voor veel verwarring en onduidelijkheid bij zowel veehouders als dierenartsen.
MycoSTOP werkt daarom aan een betrouwbaar aankoopprotocol om individuele (drager)dieren met een infectie op te sporen. Er worden specifieke protocollen uitgewerkt voor zowel kalveren als volwassen melk- en vleesvee. De kiem kan opgespoord worden via stalen zoals neusswabs, longspoelingen, vaginale swabs en melk. Bovendien zijn er in Vlaanderen reeds een heel arsenaal aan testen beschikbaar (onder andere cultuur, PCR of nanosequencing) om actieve infecties aan te tonen. Helaas kunnen intermitterende uitscheiding – waarbij dieren de kiem niet voortdurend maar met tussenpozen uitscheiden – en dragerdieren leiden tot een vals negatief resultaat, waardoor deze dieren gemist kunnen worden. Het doel van het project is dan ook om op zoek te gaan naar de meest economisch verantwoorde en betrouwbare testcombinatie.

Hoe kan ik mijn bedrijf testen op mycoplasma?
Het identificeren van individuele (drager-)dieren is een eerste stap, maar biedt onvoldoende inzicht in het risico op bedrijfsniveau – een belangrijk gemis binnen de sector. Daarom richt het tweede doel van het project zich op de ontwikkeling van een testmethode die de M. bovis-bedrijfsstatus bepaalt. Deze risicoscreening helpt veehouders inschatten wat de impact van M. bovis op hun bedrijf is en ondersteunt hen om insleep op hun bedrijf te voorkomen.
Recent onderzoek liet zien dat het testen van tankmelk een eerste belangrijke stap kan zijn, al blijven grenswaarden en interpretatie onduidelijk. De kernboodschap is dan ook dat kalveren steeds in het onderzoek moeten meegenomen worden.
Samengevat
De hoge prevalentie van M. bovis op Vlaamse melk- en vleesveebedrijven zorgt voor veel problemen en discussies. Hoewel snelscan longechografie en geavanceerde labotechnieken de diagnose verbeteren, blijft therapiefalen een hardnekkig probleem en ontbreken betrouwbare testen om dragers te identificeren. MycoSTOP werkt aan een betrouwbaar aankoopprotocol en aan strategieën voor het bepalen en monitoren van de bedrijfsstatus.





